Существует также зависимость от объема капель жидкости. Более крупные капли насыщают помещение быстрее, чем мелкие. Какова относительная влажность воздуха, насыщенного водяным паром? В этой статье вы узнаете, при какой температуре водяной пар становится насыщенным.
Прежде чем говорить о насыщенных парах, необходимо подтянуть свои знания об инертных состояниях и фазовых переходах между ними. Если вы забыли, что такое концентрированные состояния, вы можете прочитать о них в нашей статье.
При изменении внешних условий (например, когда внутренняя энергия тела увеличивается или уменьшается вследствие нагревания или охлаждения) могут происходить фазовые переходы, то есть изменения общего состояния материи.
Это могут быть фазовые переходы:
- Переход из твердого состояния в жидкое — плавление;
- Переход из жидкого состояния в твердое — кристаллизация;
- Переход из газообразного состояния в жидкое — конденсация;
- Переход из жидкого состояния в газообразное — парообразование;
- Переход из твердого состояния в газообразное, минуя жидкое — сублимация;
- Переход из газообразного состояния в твердое, минуя жидкое — десублимация.
На диаграмме показаны названия всех фазовых переходов:
Фазовые переходы — важная вещь. Вся жизнь на Земле существует только потому, что вода умеет превращаться в лед или пар. Многие процессы в металлургии и микроэлектронике включают кристаллизацию, плавление, парообразование и конденсацию.
Бесплатный урок для современных мам и пап от Екатерины Мурашовой. Зарегистрируйтесь и примите участие в розыгрыше 8 уроков

Парообразование
Таким образом, испарение — это переход из жидкого состояния в газообразное.
При испарении всегда поглощается энергия: Для того чтобы испарить вещество, к нему необходимо подвести тепло. Это увеличивает внутреннюю энергию вещества.
Процесс парообразования имеет два варианта: Испарение и кипение.
- Испарение — это превращение или переход жидкости в газ (пар) со свободной поверхности жидкости. Если поверхность жидкости открыта и с нее начинается переход вещества из жидкого состояния в газообразное, это будет называться испарением.
- Кипение — процесс интенсивного парообразования, который происходит в жидкости при определенной температуре.
Например, мы вскипятили горячий чай. Над чашкой будет виден пар, потому что вода только что прошла процесс кипения.
Минуточку, мы не говорили, что кипение и испарение — это разные вещи. 🤔 Это правда, но оба процесса могут происходить параллельно.
Испарение может происходить и без кипения, просто оно не ощутимо для нас. Например, вода в озере испаряется, хотя мы этого не замечаем. Кипение — это, по сути, интенсивное испарение, вызванное внешними условиями, которое доводит вещество до точки кипения.
Физика объясняет испарение тем, что жидкость обычно немного холоднее, чем окружающий ее воздух, и из-за разницы температур происходит испарение.
При отсутствии внешних воздействий испарение жидкостей происходит крайне медленно. Молекулы покидают жидкость благодаря эффекту диффузии.
Направление тепловых потоков при испарении может следовать различным последовательностям и комбинациям:
- из глубины жидкости к поверхности, а затем в воздух;
- только из жидкости к поверхности;
- к поверхности из воды и газовой среды одновременно;
- к площади поверхности только от воздуха.
Давайте подытожим, в чем заключается основное различие между испарением и кипячением, чтобы не запутаться:
Температура кипения
При температуре кипения давление насыщенных паров равно внешнему давлению жидкости, которое обычно равно атмосферному давлению. Таким образом, чем выше внешнее давление, тем выше температура, при которой пар имеет постоянную температуру.
Занимайтесь 15 минут в день. Освоить английскую грамматику и лексику. Сделайте язык частью своей жизни.
При сжатии насыщенного пара, температура которого поддерживается постоянной, равновесие сначала нарушается: плотность пара увеличивается, так что больше молекул переходит из газа в жидкость, чем из жидкости в газ; это продолжается до тех пор, пока концентрация пара в новом объеме не станет равной концентрации насыщенного пара при данной температуре (и равновесие восстановится). Это объясняется тем, что количество молекул, покидающих жидкость в единицу времени, зависит только от температуры.
Поэтому концентрация молекул насыщенного пара при постоянной температуре не зависит от их объема.
Поскольку давление газа пропорционально концентрации его молекул, давление насыщенного пара не зависит от занимаемого им объема. Давление p

Давление насыщенного пара .
при котором жидкость находится в равновесии со своими парами, называется давлением насыщенного пара.
При сжатии насыщенного пара большая его часть переходит в жидкое состояние. Жидкость занимает меньший объем, чем пар той же массы. В результате объем пара уменьшается, а его плотность остается неизменной.
Для идеального газа давление при постоянном объеме линейно зависит от температуры. Для насыщенных паров с давлением p0эта взаимосвязь выражается уравнением:
Поскольку давление насыщенного пара не зависит от объема, оно также зависит только от температуры.
Зависимость давления насыщенного пара от температуры.
Экспериментально определенная зависимость p0(T) отличается от зависимости ( p
=nkT ) для идеального газа.
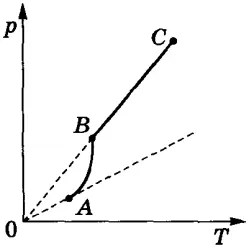
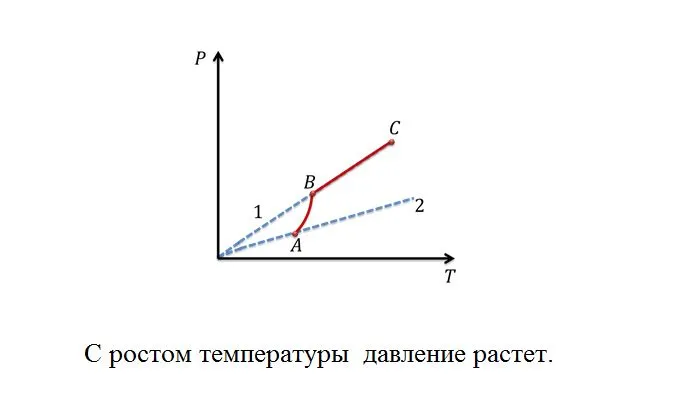
С повышением температуры давление насыщенного пара растет быстрее, чем давление идеального газа (часть кривой AB на рисунке). Это становится особенно ясно, если провести изохорду через точку А (пунктирная линия), поскольку при нагревании жидкости часть ее превращается в пар, и плотность пара увеличивается. Поэтому, согласно формуле ( p0=nkT ), давление насыщенного пара увеличивается не только из-за повышения температуры жидкости, но и из-за увеличения концентрации молекул (плотности) пара. Основное различие в поведении идеального газа и насыщенного пара заключается в изменении массы пара при изменении температуры при неизменном объеме (в закрытом сосуде) или изменении объема при постоянной температуре. Ничего подобного не может произойти с идеальным газом (молекулярно-кинетическая теория идеального газа не предсказывает фазовый переход от газа к жидкости).0После испарения всей жидкости поведение пара соответствует поведению идеального газа (часть BC кривой на рисунке выше).
Если в0Поэтому молекулы постоянно уходят и возвращаются. Если молекул вылетает больше, чем возвращается, жидкость испаряется. Если, с другой стороны, молекул возвращается больше, чем выходит, происходит конденсация. Если число уходящих молекул равно числу возвращающихся, то между веществом и паром существует так называемое динамическое (подвижное) равновесие. Пар, находящийся в равновесии с жидкостью (веществом), называется насыщенным паром.
Насыщенные пары, содержащие капельки жидкости, называются влажными парами, а ненасыщенные — сухими парами. Состояние сухого пара неустойчиво: при малейшем приложении тепла он частично конденсируется и становится жидкостью, а при приложении тепла превращается в перегретый пар.
Ненасыщенный пар.
Состояние динамического равновесия воды при комнатной температуре достигается, когда 10 22 молекул с 1 см2 поверхности воды покидают жидкость и возвращаются обратно в течение 1 секунды.
Когда скорость испарения превышает скорость конденсации, пар считается ненасыщенным и динамическое равновесие не достигается.
Рассмотрим некоторые свойства паров на примере воды и ее паров в замкнутом объеме. Наблюдения и эксперименты показывают, что давление насыщенного пара остается постоянным при постоянной температуре. Состояние насыщения означает, что достигнутая концентрация молекул воды и, следовательно, плотность насыщенного пара p
Какой пар называется насыщенным
плотность насыщенного пара p не изменяется. Когда объем начинает сжиматься (уменьшаться) при постоянной температуре, начинается конденсация и равновесие нарушается. В первый момент плотность водяного пара увеличивается, конденсируется больше, чем испаряется, пока снова не будет достигнуто равновесие. При динамическом равновесии концентрация молекул и плотность пара возвращаются к своим прежним значениям.

Поэтому при данной температуре давление пара Pnp не может превышать значение давления насыщенного пара Pnp.
Рисунок 3. Зависимость давления насыщенных паров от температуры.
При повышении температуры давление насыщенного пара быстро увеличивается, что вполне объяснимо, поскольку в результате испарения одновременно увеличивается как скорость молекул пара, так и их количество (концентрация).
Свойства насыщенного пара
Значения давления насыщенных паров при различных температурах определяются для большинства веществ путем специальных измерений. Эти данные обобщены в справочных таблицах, которые доступны как в печатном виде, так и на соответствующих веб-сайтах. Пример такой таблицы для воды и ртути приведен ниже.нпДавление насыщенных паров воды и ртути при различных температурах
Температура, 0 C
Давление паров воды,
Давление водяного пара ртути,
Таблицы свойств насыщенных паров
Температура, 0 C