Здесь реагируют простые и сложные вещества, образуются простые и сложные вещества, причем простое вещество замещает некоторые атомы сложного вещества:
Физика (7 класс)/Начальные сведения о веществе
Еще 2 500 лет назад некоторые ученые строили догадки о структуре материи. Греческий ученый Демокрит (460-370 гг. до н.э.) считал, что вся материя состоит из мельчайших частиц. Эта идея стала научной теорией только в XVIII в., а концепция строения материи была разработана лишь в XIX в. Развитие концепции строения материи позволило не только объяснить многие явления, но и предсказать, как они будут развиваться при определенных условиях.
Многие эксперименты подтверждают концепцию строения материи. Давайте рассмотрим некоторые из них.
Попробуйте сжать теннисный мяч. Это уменьшит объем воздуха в шаре. Объем надувного шарика или куска воска также можно уменьшить, приложив определенную силу.
Объем тела также изменяется при его нагревании или охлаждении.
Давайте проведем эксперимент. Возьмем медный или латунный шарик, который проходит через кольцо, когда оно не нагрето. Когда шар нагревается, он не может пройти через кольцо, расширяясь. Через некоторое время шарик, охладившись (и тем самым уменьшившись в размерах) и частично нагрев (и тем самым расширив) кольцо, снова пройдет через него.
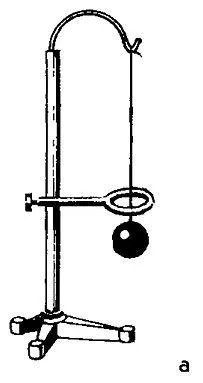
На этой фотографии видно, что латунный шарик легко проходит через кольцо, когда оно не нагрето.
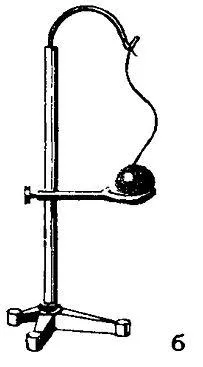
Здесь мы видим, что в нагретом состоянии, после расширения, он не проходит через кольцо, а задерживается.
С помощью эксперимента мы хотим выяснить, как изменяется объем жидкости при ее нагревании.
Плотно закройте пробкой бутылку, наполненную до краев водой. Пропустите стеклянную трубку через пробку. Вода частично заполнит трубку. Следите за уровнем жидкости в пробирке. Когда вы нагреете бутылку, вы заметите, что через некоторое время уровень воды в ней поднимется.
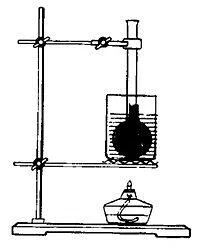
Вода не нагревается и лишь частично заполняет трубку. Уровень воды в трубе низкий.
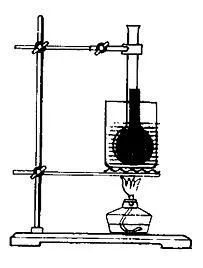
Вода нагрелась, расширилась и заполнила свободное пространство. Уровень воды в трубе повысился.
Таким образом, объем тела увеличивается при нагревании и уменьшается при охлаждении.
Давайте попробуем объяснить, почему изменяется объем тела.
Очевидно, что все вещества состоят из отдельных частиц с промежутками между ними. Когда частицы удаляются друг от друга, объем тела увеличивается. А когда частицы сближаются друг с другом, объем тела уменьшается.
Тогда возникает вопрос: если тело состоит из мельчайших частиц, почему оно кажется нам твердым?
Современная наука доказала, что Т
Если бы вы смогли уложить 10 000 000 (или 10-7 градусов) молекул воды вплотную друг к другу, у вас получилась бы нить длиной всего 2 мм. Малый размер молекул позволяет создавать тонкие слои различных веществ. Например, капля масла может растечься по воде тонким слоем толщиной 0,000002 м (или 2 в степени 10-6).
Даже маленькие тела состоят из огромной массы молекул. Например, крупинка соли или сахара содержит очень большое количество молекул. Считается, что в 1 см³ воздуха содержится примерно от 27 до 1018 молекул степени. Чтобы понять, насколько велико это число, представьте следующее. Один миллион молекул в секунду проходит через небольшое отверстие в воздухе. Указанное количество молекул пройдет через отверстие в течение следующих 840 000 лет.
Молекулы. править
Из-за своего очень маленького размера молекулы невидимы для невооруженного глаза или обычного микроскопа. Но с помощью специального прибора, электронного микроскопа, удалось сфотографировать самые крупные из них. На рисунке показано расположение молекул белка.

Тела вокруг нас, даже если на первый взгляд они похожи, будут отличаться. В природе вы не найдете двух одинаковых снежинок или песчинок, людей, животных и т.д., которые выглядели бы совершенно одинаково.
Ученые доказали с помощью экспериментов, что молекулы разных веществ различны, а молекулы одного и того же вещества одинаковы. Например, воду, полученную из сока или молока, невозможно отличить от воды, полученной путем дистилляции из морской воды. Молекулы воды одинаковы. Никакое другое вещество не может состоять из таких молекул.
Молекулы, с другой стороны, состоят из еще более мелких частиц, называемых атомами.
Например, самая маленькая частица воды — это молекула воды. Он состоит из трех атомов: двух атомов водорода и одного атома кислорода. Из курса химии вы знаете, что вода называется H2O. H — атом водорода, а O — атом кислорода.
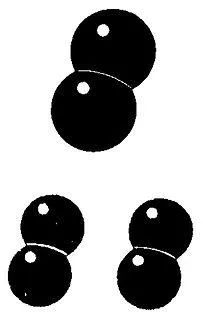
Молекулы обычно представляются схематически, т.е. с помощью молекулярных моделей. На рисунке изображены две молекулы воды. При разделении двух молекул воды образуются два атома кислорода и четыре атома водорода. На следующем рисунке показано, что любые два атома водорода могут соединиться вместе и образовать молекулу водорода, а атомы кислорода могут соединиться вместе и образовать молекулу кислорода.
Атомы также состоят из более мелких частиц, но об этом вы узнаете на уроках химии в 8 классе.
Хорошо известно, что если поместить в комнату пахучее вещество, например, духи или нафталин, то вскоре запах будет ощущаться во всем помещении. Распространение запахов происходит благодаря тому, что молекулы духов (или нафталина) находятся в движении.
Поэтому возникает вопрос, почему запах распространяется в помещении не сразу, а только через некоторое время.
Причина в том, что движению молекул парфюма в определенном направлении препятствует движение молекул воздуха. Молекулы духов (или нафталина) на своем пути сталкиваются с молекулами газа, входящего в состав воздуха. Они постоянно меняют направление и летят сквозь пространство в своих беспорядочных движениях.
Давайте проведем опыт, который можно объяснить только тем, что тела состоят из молекул, которые движутся в
Наблюдаемое явление объясняется тем, что молекулы воды и сульфата меди, находящиеся вблизи границы раздела этих жидкостей, обменялись своими позициями. Интерфейс стал размытым. Молекулы сульфата меди попали в нижний слой воды, а молекулы воды переместились в верхний слой сульфата меди.

Если оставить стекло на 2-3 недели, граница между ними станет еще более размытой и постепенно исчезнет совсем. Вся вода станет синей. Это происходит потому, что молекулы, которые движутся непрерывно и беспорядочно, распределяются по всему объему. Жидкость в емкости становится однородной.
Диффузия в газах, жидкостях и твердых телах. править

Явление взаимного проникновения молекул одного вещества между молекулами другого вещества называется диффузией.
Диффузия также происходит в твердых телах, но с еще более медленной скоростью.
Например, очень гладко отполированные пластины из свинца и золота кладут друг на друга и взвешивают. (При комнатной температуре (20 °C) золото и свинец диффундируют друг через друга за 4-5 лет на расстоянии около 1 мм. Во всех описанных выше экспериментах наблюдается взаимное проникновение молекул веществ, т.е. диффузия.
Явление диффузии играет важную роль в природе. Диффузия, например, поддерживает однородный состав атмосферного воздуха у поверхности Земли. Диффузия солей в почве приводит к нормальному питанию растений и т.д.
Золото, ювелирные изделия, монеты из золота, серебра, серы из вулканических источников, железа и меди известны уже тысячи лет. Ученые древности пытались объяснить его структуру. Демокрит создал атомизм, Аристотель стал «основателем» современного естествознания. Ученые развили идею materia prima в виде пяти первоэлементов или стихий: Воздух, Вода, Земля, Огонь и Эфир.

Материя или вещество рассматривалась древними как нечто, «из чего что-то сделано». Возникла идея о существовании очень маленьких частиц — атомов. В переводе с греческого этот термин означает «неделимый».
Изучение частиц почти как детективная история. Выдающийся русский ученый М. Ломоносов часто использовал термины «частица», «атом», «атомы» и «молекула». Все было очень запутанно: атомы делимы или нет, что из чего состоит?
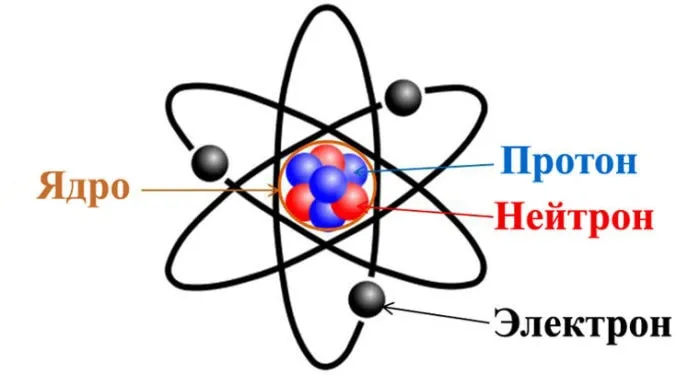
Согласно решению Международного конгресса химиков в 1860 году, атом — это мельчайшая частица, из которой состоит простое или сложное вещество. Молекула — это система ядер и электронов двух или более атомов. Частицы, невидимые невооруженным глазом, можно увидеть только под большим увеличением электронного микроскопа.
Атомы состоят из ядер и электронов. Первые заряжены положительно. На близком расстоянии отрицательно заряженные электроны движутся с большой скоростью. Ядра содержат элементарные частицы: протоны (положительные), нейтроны (отрицательные).
Если число протонов равно
Интересный факт: атомы Na, K, Ca и Cl опасны для жизни, если попадают в организм вместе с пищей. Ионы Na+, K+, Ca2+ и Cl безопасны и жизненно необходимы для организма.
Будет ли чай в стакане слабым, если не размешать сахар? Да, конечно. Но через некоторое время молекулы сахара поднимаются со дна стакана в верхние слои жидкости. Так движутся молекулы. Как они перемещаются и куда?
Знать, что «из чего сделано»
Простой эксперимент:
Если вы положите полчашки гороха в полчашки булгура, не перемешивая, то получите целую чашку. Булгур и горох мелкие, но их нельзя «втиснуть» в пустые пространства.
Вещества — скопления очень маленьких компонентов
Что произойдет, если в мензурку налить равные количества воды и спирта? Не происходит удвоения смеси, как в первом случае. Почему бы и нет? Молекулы воды и спирта совершенно разные. Между молекулами воды больше промежутков, чем между молекулами спирта. Эти промежутки частично заполняются, что уменьшает объем смеси.

Таким же образом молекулы сахара «распределяются» по всему объему, делая чай сладким.
Атомы, изотопы
(Источники 1 и 2)
Проникновение молекул одного вещества в промежутки между молекулами другого вещества называется диффузией.
В газах диффузия также является довольно распространенным процессом. Когда вы проходите мимо фабрики сладостей, вы чувствуете запах конфет, зефира или шоколада; когда вы входите в парикмахерскую, вы чувствуете запах духов, одеколона или туалетной воды. Людей постоянно сопровождают запахи. Благодаря диффузии они несут важную информацию о веществе. В газах диффузия происходит быстрее, чем в жидкостях, и вот почему. Межмолекулярные расстояния в газах больше, чем в жидкостях, поэтому возможность движения больше.
- идентичностью частиц одного вещества;
- наличием разных структурных единиц (атомов, молекул, ионов);
- отличиями зарядов, масс и размеров видов атомов (химических элементов);
- способностью атомов и молекул терять или приобретать электроны, превращаясь в ионы — заряженные частицы;
- огромным количеством электронных конфигураций, кристаллических структур;
- различиями в энергетическом состоянии частиц.
Но возможна ли диффузия в твердых телах? Мы должны учитывать, что твердое тело сохраняет свою форму благодаря расстояниям, близким или даже меньшим, чем размер самих молекул. Могут ли туда проникнуть «чужие» молекулы? Было установлено, что диффузия возможна и в твердых телах, но только в том случае, если они находятся в очень тесном контакте друг с другом. Процесс идет очень медленно, и время измеряется годами. Хорошо известен эксперимент с двумя полированными телами из золота и свинца. Они были тесно прижаты друг к другу и помещены под наблюдение. Была диффузия. Только на 1 мм за пять лет.
Движение молекул
(Источник)
Движение молекул и промежутков между ними объясняет диффузию. Впервые эта гипотеза была сформулирована в III веке до н.э. греческим ученым Эпикуром.
Это было экспериментально доказано в 1827 году Броутоном, известным английским ботаником. Он рассматривал споры растения подорожника в воде под микроскопом и заметил, что эти маленькие частицы постоянно двигались в разных направлениях. Неустанное, хаотичное движение продолжалось весь день и всю ночь.
Из-за комбинаций атомов разные вещества имеют разные молекулы. А если посмотреть на одно и то же вещество в разных ситуациях, например, на воду из крана, в чашке чая или в ручье. Во всех трех случаях молекулы одинаковы, но ведут себя по-разному. В горячем чае молекулы движутся быстрее. В холодном потоке они движутся гораздо медленнее. А в водопроводной воде молекулы движутся медленнее, чем в горячем чае, но быстрее, чем в ручье.

Конечно, речь идет о скоростях, на которых человек не может двигаться. Человек может бежать со скоростью 4 — 7 км/ч. Скорость молекулы воды при комнатной температуре составляет в среднем 590 м/с = 2124 км/ч (в кипящей воде — ≈ 2340 км/ч). Это можно понять, если сказать, что одни молекулы движутся быстро, а другие медленно.

Когда они говорят «холодно», «жарко», «горячо», они сравнивают температуру. Температура тела определяется тем, как движутся молекулы этого тела: быстро или медленно. Чем выше температура, тем быстрее движутся молекулы. Если молекулы движутся медленнее, температура тела снижается.
Природа вокруг нас зависит от температуры. С понижением температуры наступает осень, а затем зима. Когда температура повышается, зима уступает место весне, а весна — лету.
Свойства материи также зависят от температуры. Например, мягкая резина затвердевает на холоде, а твердый лед становится жидким, если его занести в теплое помещение.
Температура характеризует свойства живых и неживых существ. Поэтому о нем можно многое узнать. Самое главное: скорость движения молекул, из которых состоит вещество, определяет его температуру.

Для измерения температуры используются приборы — термометры. Термометры изготавливаются в зависимости от их назначения:
Температура измеряется в градусах. В 1742 году шведский геолог, метеоролог и астроном Андрес Келсос изобрел шкалу, основанную на точках отсчета: точке плавления льда (0 градусов) и точке кипения воды (100 градусов).
(Источник)
В 1848 году Уильям Томпсон (лорд Кельвин) ввел понятие абсолютного нуля температуры (-273 градуса, самая низкая температура во Вселенной). Так, температура плавления льда составляет уже 273 градуса, а температура кипения воды — 373 градуса.
Для измерения температуры используются приборы — термометры. Термометры изготавливаются в зависимости от их назначения:
В 1724 году польско-немецкий ученый Даниэль Габриэль Фаренгейт создал свою шкалу, которая стала использоваться в англоязычных странах. Он до сих пор используется только в Соединенных Штатах.
Температура
(Источник)
Все три шкалы основаны на двух угловых точках — температуре, при которой выбранное вещество переходит из одного состояния в другое.
В шкалах Цельсия и Кельвина вода имеет температуру au
Молекулы прочно удерживаются вместе. И если вы попытаетесь сложить две части сломанного куска дерева вместе, он не станет целым. Таким образом, между молекулами существует постоянная связь (взаимодействие).
Благодаря притяжению молекул и атомов, тела не распадаются на отдельные частицы. Если бы, с другой стороны, существовало только межмолекулярное притяжение, то между молекулами не было бы никаких промежутков, но они есть. Следовательно, должно существовать и отталкивание. Однако это происходит только тогда, когда зазор между молекулами меньше, чем расстояние между молекулами. Чем ближе молекулы движутся, тем сильнее они отталкиваются друг от друга.
В случае со сломанной палкой края обломков разрушились, и вы не можете просто свести их одной рукой до такой степени, чтобы молекулы начали взаимодействовать. Поэтому результат эксперимента будет равен нулю.
А теперь еще один эксперимент. Вам нужно разделить два листа стекла, которые лежат друг на друге.
- лабораторные;
- медицинские;
- уличные;
- комнатные;
- технические.
- жидкостные;
- газовые;
- механические;
- электрические;
- оптические.
Это нелегко сделать. Почему бы и нет? Догадаться об этом несложно. Молекулы двух пластин находятся довольно близко друг к другу, потому что пластины очень гладкие. Происходит взаимодействие (молекулярное притяжение).
Для измерения температуры используются приборы — термометры. Термометры изготавливаются в зависимости от их назначения:
Между жидкостью и твердым телом существует взаимное притяжение. Это называется смачиванием. Например, вода смачивает многие ткани, дерево и бумагу, но не притягивается к пластилину, воску и жирным поверхностям. Этот процесс называется несмачиванием. Смачивание и несмачивание встречаются в повседневной жизни, в технике, в живых и неживых существах.

Для измерения температуры используются приборы — термометры. Термометры изготавливаются в зависимости от их назначения:
Что такое химия? Где мы находим химические явления? Везде. Сама жизнь — это мириады различных химических реакций, благодаря которым мы дышим, видим голубое небо, чувствуем запах прекрасных цветов…..

Для измерения температуры используются приборы — термометры. Термометры изготавливаются в зависимости от их назначения:
Понятно, что такое вещество: это то, из чего состоит мир вокруг нас и мы сами. Но что такое химический процесс (явление)?
Химические явления — это процессы, которые изменяют состав или структуру молекул, составляющих определенное вещество. Молекулы изменились — вещество изменилось (стало другим!) — его свойства изменились:
Все эти изменения являются результатом сложных и разнообразных химических процессов. Итак,
Взаимодействие молекул
Химия — это наука о веществах и их превращениях.

Не все преобразования изучены,
Число атомов в молекуле обозначается индексом:
Если атомы не связаны химически, то количество атомов обозначается коэффициентом:
Число молекул представлено таким же образом:

Почему атомы водорода и кислорода имеют разные названия, разные символы? Потому что они являются атомами разных химических элементов.
Химический элемент состоит из частиц с одинаковым зарядом в ядрах их атомов.
Что представляет собой ядро атома? Почему заряд атомного ядра является показателем принадлежности атома к определенному химическому элементу? Чтобы ответить на эти вопросы, необходимо их прояснить: Изменяются ли атомы во время химических реакций? Из чего состоит атом?
Существуют простые и сложные вещества. Если молекула состоит из атомов одного химического элемента, то это простое вещество:


- Между молекулами действует взаимное притяжение и отталкивание
- Величина притяжения и отталкивания определяется расстоянием между молекулами
- Взаимодействовать друг с другом могут молекулы и атомы различных веществ
Урок 1. Основные понятия и законы предмета «Химия»
Если вещество состоит из атомов только одного химического элемента, то это простое вещество. А некоторые химические элементы образуют различные простые вещества. Например, химический элемент кислород образует простое вещество «кислород» O
и простое вещество «озон» O
* В 2002 году было сообщено, что существует еще одно простое вещество — кислород O.
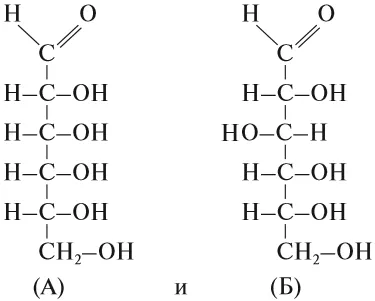
А химический элемент углерод образует четыре простых вещества, ни одно из которых не называется «углерод». Эти вещества отличаются пространственным расположением своих атомов:
- свежее молоко стало кислым;
- зелёные листья стали жёлтыми;
- сырое мясо при обжаривании изменило запах.
В четвертой модификации «углерода», фуллерене, атомы углерода образуют сферу, то есть молекулы фуллерена выглядят как сфера.
Наличие элемента в виде нескольких простых веществ называется аллотропией. Алмаз, графит, карбин, фуллерен являются аллотропными модификациями элемента «углерод», а кислород и озон — аллотропными модификациями элемента «кислород».
Поэтому не следует путать термины «химический элемент» и «простое вещество», а также «молекула» и «атом».
- обязательно изменяется состав или строение молекул;
- никогда не изменяется состав и заряд ядер атомов.
В письменном виде слова «молекула» или «атом» очень часто заменяются соответствующими символами, но не всегда правильно. Например, неправильно писать: «Вода содержит H
» при упоминании химического элемента водорода — H. Правильно писать: «Вода содержит ( Н )». Соответственно, правильной записью будет: «Когда металл действует в кислом растворе, H
«, т.е. вещество водород, молекула которого является двухатомной.
Сложные молекулы состоят из атомов различных химических элементов:
Как мы знаем, соединения состоят из атомов различных химических элементов. Эти атомы соединены друг с другом химическими связями: ковалентными, ионными и металлическими.
Способность атома образовывать определенное количество ковалентных химических связей называется валентностью. (Для получения дополнительной информации см. урок 4, «Химический контейнер

- О2— это молекула вещества кислорода, состоящая из двух атомов кислорода;
- Н2О — это молекула вещества воды, состоящая из двух атомов водорода и одного атома кислорода.
Вещества, состав которых отражает химические типы, могут участвовать в химических процессах (реакциях). Графическое представление конкретной химической реакции называется уравнением химической реакции. Например, при сжигании угля (в сочетании с кислородом) происходит химическая реакция:
Запись показывает, что атом углерода C соединяется с молекулой кислорода O
- 2Н2— две молекулы водорода;
- 3Н2О — три молекулы воды.
с образованием молекулы углекислого газа CO
. Количество атомов отдельных химических элементов до и после реакции должно быть одинаковым! Это правило является следствием закона сохранения массы: масса исходных материалов равна массе продуктов реакции. Закон был открыт в XVIII веке М.В. Ломоносовым и, независимо от него, А.Л. Лавуазье.
При применении этого закона коэффициенты должны быть вставлены в уравнения химических реакций таким образом, чтобы число атомов каждого химического элемента не изменялось в результате реакции. Например, при разложении соли хлорида берилла KClO.
Простые и сложные вещества. Валентность
вы получаете соль KCl и кислород O
Число атомов калия и хлора одинаково, но число атомов кислорода различно. Давайте поставим их в равные условия:2Теперь количество атомов калия и хлора изменилось до начала реакции. Давайте поставим их в равные условия:3*.
Теперь мы можем поставить знак равенства между правой и левой частями уравнения:4.
Полученный символ показывает, что разложение двух молекул KClO
- Алмаз — атомы углерода находятся в вершинах воображаемых тетраэдров;
- Графит — атомы углерода находятся в одной плоскости;
требуется две молекулы КСІ и три молекулы кислорода O
. Количество молекул задается коэффициентами.
При выборе коэффициентов нет необходимости считать отдельные атомы. Если состав определенных групп атомов не изменился в ходе реакции, то количество этих групп можно рассматривать как единое целое:
Последовательность операций следующая:21. определить прочность исходных атомов и группы PO.22. перенесите эти числа в правую часть уравнения:
3. написать химические формулы полученных веществ в соответствии со значениями составляющих компонентов:
4. укажите состав «самого сложного» соединения: Ca
(PO
и поставить число атомов кальция (их три) и число PO
(их два):25. Число атомов натрия и хлора до реакции теперь равно шести; добавим соответствующий коэффициент:
Эти правила составляют алгоритм уравнений реакций химического обмена, поскольку с помощью этой последовательности можно уравнять схемы многих химических реакций, за исключением более сложных окислительно-восстановительных реакций (см. урок 7).
Уравнения химических реакций
Существует несколько типов химических реакций. Наиболее важными из них являются:
1. большинство сложных реакций являются сложными реакциями:2Здесь вещество образуется из двух или более веществ:22. 1. Реакции разложения:
32:
32
4:
34)24